
伴随着新型冠状肺炎病毒在全球范围内肆虐传播,短时间疫情在各国迅速爆发、升级,不少国家相继宣布公共卫生系统进入紧急状态。同时也引发了各国民众因生活物资短缺而产生的焦虑、恐慌,其中医疗防疫物资短缺带来的影响最为显著。
目前,中国的疫情发展已逐步稳定,生产生活也开始渐渐恢复,作为口罩年产量占全球约50%的世界最大口罩生产和出口国,中国在此次抗疫行动中,加大力度提升相关防疫医疗器械的产能水平,中国目前口罩日产量已经可以达到1.16亿只,医用N95口罩日产量达到166万只,医用防护服日产量超过30万件(截至2月29日的数据)。
我国在保证国内医疗物资补给充足的同时,也有大国担当,积极向其他受疫情困扰的国家及地区提供最大力度的援助和支持。在国内疫情初步稳定后,我国继续投入巨大的人力物力财力资源用于紧急生产出口供他国防疫的医疗物资。根据中国外交部3月31日公开的数据,中国政府已向120个国家和4个国际组织提供了包括普通医用口罩、N95口罩、防护服、核酸检测试剂盒、呼吸机等在内的物资援助。此外,中国地方政府也通过国际友好城市等渠道向50多个国家捐赠了医疗物资。部分中国企业也向100多个国家和国际组织捐赠了医疗物资。商业方面,已有30个国家和2个国际组织同中方出口商签署了包括口罩、防护服、核酸检测试剂在内的商业采购协议,并有多国采购商正同中国企业治谈合作。[1]
在中国为全球抗击疫情行动做出巨大努力时,却有不少国家对此发出了质疑的声音,主要是针对中国输出的医疗防疫产品质量问题。据外媒3月28日(当地时间)报道,荷兰政府以不满足品质要求为由,召回了从中国进口的130万个口罩。荷兰政府称,该批口罩在第一轮质量测试中证实未达标,并且第二次测试也未能满足标准,因此决定全部不予使用。荷兰政府还表示,今后将对从中国追加进口的产品也进行彻底检查。此外,在菲律宾也出现了指责中国生产的新型冠状肺炎检测试剂盒的准确度存在问题的声音。菲律宾卫生保健部称,中国捐赠的检测试剂盒中一部分产品的检测准确率仅仅能达到40%。而中国政府向菲律宾捐赠的试剂盒数量达10万余个之多。此前,西班牙也曾公布称,从中国深圳生物科技有限公司进口的试剂盒的检测准确率不到30%。
随着这类案例的增多,由中国出口的防疫物资的质量水平不断受到海外舆论质疑,致使中国相关生产企业的口碑和声誉均遭受到了不良影响。更直接的结果是我国企业生产出口的大批防疫物资因不符合进口国准入标准而长时间积压在海关无法输出,甚至被订购方退货、索赔、取消后续订单。这对疫情期间增加投入、扩大生产的相关医疗物资制造出口企业而言无疑是重大的打击。在此情况下,我们亟需结合各输入国家及地区对医疗防疫物资的质量标准要求,对我国防疫医疗物资的出口监管标准进行明确和优化,从而减少壁垒,畅通贸易,在积极加强与海外合作的同时保障我国相关医疗物资生产企业的合法权益,降低交易过程中可能产生的法律风险,避免承担不必要的违约责任。
一. 出口防疫物资的企业资质要求
疫情之下,有大批外贸出口企业都转而加入了口罩生产、销售的行列。中国外交部发言人华春莹在3月30日的例行记者会上表示,“我们在保证国内防疫需求的前提下,支持有资质、有信誉的企业对外出口,并在生产、运输、清关各个环节为各国来华采购和企业有序地出口提供便利。”商务部也在3月30日发布消息,称将会同相关部门严把质量关,维护出口秩序,严厉打击假冒伪劣行为。为此中国商务部、海关总署、国家药品监督管理局于3月31日联合发布《关于有序开展医疗物资出口的公告》,“自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得中国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。”在此新规出台之前,我国原本的规定只要求有海外销售资质(例如获得欧盟CE认证)即可出口物资。这就致使一些中国企业利用该规定,在未得到中国政府批准时就可以将物资出口至海外。现在的新规无疑是收紧了医疗防疫物资的输出关口,以避免质量不合格产品的意外流出。但与此同时也对准备生产出口口罩等医疗防疫物资的外贸企业提高了经营资质门槛,要求其生产的产品在满足进口国家(地区)的质量要求的同时,还要取得我国医疗器械产品注册证书,再结合《生产监管办法》第七十条的规定:“我国的医疗器械生产企业接受境外企业委托,生产在境外上市销售的医疗器械的,应当取得医疗器械质量管理体系第三方认证或者同类产品境内生产许可或者备案。”,即使企业生产的检测试剂、医用口罩等防疫产品只出口至订购国,不在我国境内上市流通也需要取得医疗器械生产许可证或是办理医疗器械生产备案。
此外,对于不具备医疗器械经营资质的普通贸易公司能否从事检测试剂等防疫物资的出口,以及防疫物资出口对进出口企业是否有特殊要求等问题,海关给出的官方答复是对此无特别限制。[2]外交部也公开表示,我国不仅不会对防疫物资的出口采取外贸限制,还会大力支持企业有序地扩大出口。虽然我国海关没有特别要求,但一般情况下进口方会要求生产企业提供营业执照、医疗器械产品备案证或者注册证、厂家检测报告等相关资质证明文件,用于证明进口产品在中国是合法生产的。
二.海外医疗防疫产品的质量标准及准入流程——以口罩为例
1. 国内外对口罩产品质量的具体要求
(1)海外要求的质量标准(以下图标明的地区为例)
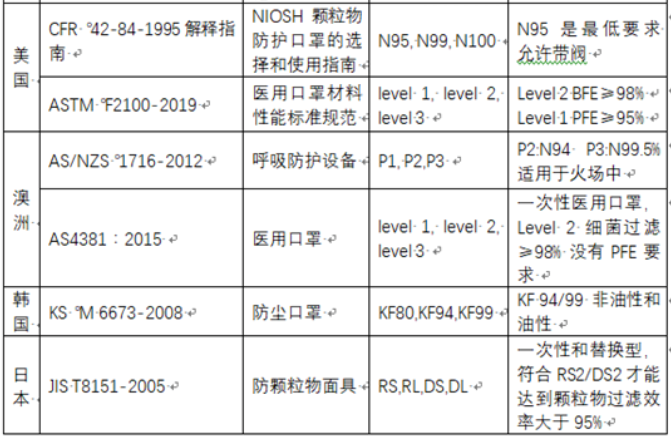
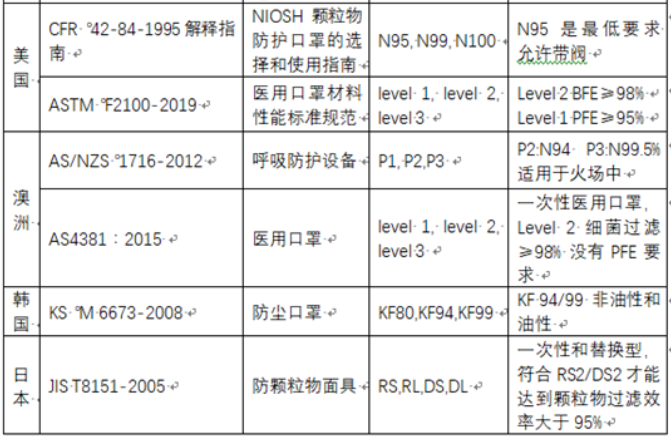
(2)国内要求的质量标准
2020年1月30日,我国国家卫生健康委员会发布了《新型冠状病毒感染不同风险人群防护指南和预防新型冠状病毒感染的肺炎口罩使用指南》,其中提到了四种推荐口罩类型,分别为:一次性使用医用口罩、医用外科口罩、KN95/N95及以上颗粒物防护口罩,还有医用防护口罩。我国对这四类用于防疫的口罩都有其对应的技术标准要求,依次为:《一次性使用医用口罩》(YY/T0969-2013)、《医用外科口罩》(YY0469-2011)、《医用防护口罩技术要求》(GB19083-2010)以及《呼吸防护用品自吸过滤式防颗粒物呼吸器》(GB 2626-2007)。
由此可见,不同国家对于口罩这一基础医疗防疫产品的具体分类及检测标准都有所区别,其中表现出了较大的差异性。这就要求此类产品的生产出口商在签订国际贸易合同前必须要对进口国家及地区的质检标准有充分的了解,使生产出口的产品完全符合输入地的要求,从而避免因国家间的质量标准差异导致的违约情形发生。
2. 医用口罩出口海外的准入流程(以欧盟、美国、日本、韩国为例)
(1)欧盟
在欧盟市场,医用口罩按照MDR(欧盟医疗器械法规)的要求须进行CE认证。医用口罩产品按照I类器械进行管理。依据产品是无菌类或非无菌类,其认证模式也有不同。
1)非无菌方式认证流程:编制技术文件——提供测试报告(可以提供熔喷布性能测试报告和无纺布的生物学报告,咨询合作的公告机构的意见)——编制DOC——指定欧盟授权代表并完成欧洲注册。
2)无菌方式认证流程:灭菌验证——建立ISO13485体系(医疗器械质量管理体系)——编制技术文件——提供测试报告(口罩本身的生物学、性能、无菌等测试报告)——公告机构审核——获CE证书——指定欧盟授权代表并完成欧洲注册。[3]
无菌医用口罩在欧盟获得认证的过程较为繁琐,还需要欧盟公告机构的参与。若医用外科无菌口罩之前没有获得过公告机构的CE证书,那么申请认证的周期可能会很长。
(2)美国
医疗器械进入美国市场可以通过豁免、510(k)、PMA三种认证形式进行。510(k)即上市前通告(Pre-market Notification),证明产品与已经合法上市的产品实质性的等同。PMA,指上市前审批(Pre-market Approval),旨在提供足够、有效的证据证明医疗器械按照设计和生产的预期用途,能够确保产品的安全有效。
同时,美国FDA(食品药品监督管理局)根据风险等级将医疗器械分为Class 1、Class 2、Class 3三类进行管理。Class 1 为普通管理产品,指危险性小或基本无危险性的产品。FDA认为绝大多数的1类产品通过一般控制足以保证其安全性和有效性。如医用手套、压舌板、手动手术器械等,一次性医用口罩就属于该类。这类产品的出口流程相对比较简单,只需填写申请表格,进行信息确认,取PIN码,交付年费,下发注册号,最后完成产品出口。
医用外科口罩被归为2类产品。属于Class 2的产品需要上市前通告,流程较为复杂,需要先进行产品测试(性能测试、生物学测试),之后准备510(k)文件,提交FDA评审,FDA发510(k)批准信,完成工厂注册和机器列名,最后实现产品出口。
N95防毒口罩是是受美国国家职业安全与健康研究所(NIOSH)中国家个人防护技术实验室(NPPTL)的监管,按照NIOSH的认证标准(42 CFR Part 84),具体要求为:送样品至NIOSH实验室实施测试,同时提交技术性资料(包括质量体系部分资料)至NIOSH文审,在文审和测试都通过后,由NIOSH核发批文,最后完成产品出口。
(3)日本
在日本口罩被划分为Ⅱ类器械(管理医疗器械)进行管理。管理医疗器械在认证基准确定的情况下,由第三方认证机构进行认证;若没有认证基准或不符合认证基准,则由PMDA(Pharmaceuticals and Medical Devices Agency)进行审评,厚生省承认。此外,日本对在本国销售医疗器械的公司要求非常严格,其必须严格遵守日本的医药品与医疗器械法令(PMD Act)相关规定。作为审批流程的一部分,医疗器械制造商必须遵守厚生劳动省与质量管理体系相关的第169号法令;任命一名本国的代理(MAH/ D-MAH);对设计与生产设施进行注册登记,并满足其他相关要求。
(4)韩国
医用外科口罩在韩国属于Ⅱ类医疗器械产品。MFDS(Ministry of Food and Drug Safety)对Ⅱ类器械要求须在上市前获得批准。韩国规定进口商也应确保进口产品符合质量管理体系的要求,并拿到MFDS授权机构的许可。申请MFDS认证需要提供的资质包括:提单、箱单、发票、韩国进口商营业执照,同时需要在韩国的收货人到韩国药监局(Korea Pharmaceutical Traders Association)提前备案进口资质。此外,MFDS还要求口罩需要有详细的原产地标识(例如,中国制造必须标注“Made in China”)、生产厂家信息、保质期,还要准备成分含量说明,制造工艺流程,此外在货物抵达韩国以后还需要进行化验,送交样品到实验室,化验合格后方可进入韩国市场销售流通。[4]
三、签订出口防疫物资国际贸易合同可能存在的法律风险及相关法律建议
1. 明确权利义务
由于各国对产品的质量要求及认证标准都有不同,因此在签订国际贸易合同时一定要对双方的权利、义务以及产品要求做出明确且具体的约定,以避免承担因约定条款模糊而可能产生的违约、侵权等法律责任。对于个别符合中国相关产品质量标准,但没有或者还来不及获取输入国家相关资质认定的产品,应提前与进口方就这一问题进行沟通,确保对方知悉相关情况。
2. 标明产品使用条款
合同中还应该对出口产品的质量要求和正确的使用规范做出明示,尤其是对于在操作上有特别注意事项的产品,更应做好充分说明,条件允许的情况下可以加强售后服务,进行跟踪反馈。若因进口方没有按照规范操作使用产品,致使产品的使用效果减弱或达不到规定标准,那么进口方无权要求出口方进行赔偿或承担违约责任。
3. 合理适用不可抗力条款
在新冠疫情蔓延的当下,将不可抗力条款约定进合同也是保障出口方权益的有力措施之一。我国规定不可抗力可以是自然原因酿成的,也可以是人为或社会因素引起的,适用情形主要包括(1)自然灾害,如台风、洪水、冰雹;(2)政府行为,如征收、征用;(3)社会异常事件,如罢工、骚乱。此次突发的疫情也应当属于不可抗力的范畴。在这一特殊情况下,合同签订双方可以通过约定不可抗力条款使无法按规定履约的一方获得免责。但需要注意的是,对于与我国分属不同法系的国家,若其没有在法律中对不可抗力进行认可,那么引用不可抗力条款也无法保障我国出口企业的权益。因此对不可抗力条款的援引还应依据签订合同双方国家的具体法律规定,酌情使用。
4. 选择适用的法律
国际贸易合同签订时还必须注意适用法的选择,须对合同双方的利益尽量权衡。在双方没有明确约定适用法律的情况下,从尽可能保护我国生产出口企业利益的角度出发,可依照《中华人民共和国涉外民事关系法律适用法》第四十五条:“产品责任,适用被侵权人经常居所地法律;被侵权人选择适用侵权人主营地法律、损害发生地法律的,或者侵权人在被侵权人经常居住地没有从事相关经营活动的,适用侵权人主营地法律或者损害发生地法律。”的规定进行归责。
5. 选择运输交付方案
因疫情扩散,运输业也深受影响。随着疫情的蔓延,各国相继出台减少、取消航班,加强出入境关口管制等政策,在严防境外输入病例的同时,也增加了国际货物交易在运输环节上的难度。运力不足致使货物运输时间无法保证,交货存在风险。因此出口方在订立合同条款时应尽量选择卖方无需在运输、清关等环节承担较重义务的交易方案,可以适当使用买方承担较多义务的术语,例如EXW(工厂交货)进行交易,从而避免承担货物在运至指定目的地之前可能产生的风险及费用。
6. 合理约定交付时间
鉴于医疗防疫物资的特殊性,不同国家对产品的质量要求差别较大,这就要求出口产品在符合国内生产标准的同时,还必须通过进口国的质量认证。如前文提到的,多数国家对医疗器械类产品的市场准入条件设定严格,认证流程繁琐复杂,出口产品要获得输入国的认证可能需要花费很长的周期。因此在签订合同时,生产出口的一方应当考虑到获得认证的困难性,在约定的产品交付时间中预留出申请认证可能需要的时长,从而避免因认证周期长,产品无法如期交付而导致的违约。
结语
新型冠状肺炎疫情的突然爆发,使世界各国都遭受到了巨大打击,对全球经济的影响更是不容小觑。中国在此次全球抗疫行动中,始终站在第一线,在稳定国内疫情之余,中国政府、企业及个人也积极向其他国家及地区出口、捐赠医疗物资,本着人类命运共同体的理念为世界各国提供力所能及的支持。但在如今脆弱的经济环境下,出口、捐赠医疗物资的企业也需要有基本的法律风险防范意识,提前规避风险,以免承担不必要的违约责任。
脚注:
[1] 防疫物资出口情况参考中国经济网微信公众号发布的《多国向中国采购防疫物资 耿爽:鼓励有序扩大出口 没有任何外贸限制措施》:
https://baijiahao.baidu.com/s?id=1662130259521204310&wfr=spider&for=pc, 2020年4月8日登入
[2] 参考雨果网微信公众号发布的《海关权威答复!外贸企业出口防疫物资是否需要经营资质?》:
https://baijiahao.baidu.com/s?id=1663168002819280970&wfr=spider&for=pc, 2020年4月8日登入
[3] 参考欧盟防护口罩认证要求:
http://www.tbtmap.cn/rdht_124/xgfyfhypzr/EUfhypzr/202003/t20200318_2283023.html,2020年4月8日登入
[4] 参考韩国医药用品进出口协会网站:
http://www.kpta.or.kr/main/main.asp,2020年4月8日登入


版权声明:本文版权归 锦天城南京律师事务所王芳高级合伙人团队 所有,转载请通过邮件和电话与锦天城律师事务所王芳高级合伙人团队取得联系

关注微信企业号
获取更多服务